EMOCLOT DI FAKTOR VIII 1000 IU 1 flakon
Bölümü
Kullanılır
Kullanılır
Etkileri
Nelerdir
EMOCLOT 1000IU/10 mL IV infüzyon için liyofilize toz içeren flakon
Damar içine uygulanır.
Etken Madde
Dondurularak kurutulmuş insan plazma kaynaklı pıhtılaşma Faktör VIII 1000 IU. EMOCLOT ‘nın spesifik aktivitesi yaklaşık 80 IU/mg proteindir.
Yardımcı maddeler
Tribazik sodyum sitrat, sodyum klorür, glisin, kalsiyum klorür, enjeksiyonluk su
Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.
Bu kullanma talimatını saklayınız. Daha sonra tekrar okumaya ihtiyaç duyabilirsiniz.
• Eğer ilave sorularınız olursa, lütfen doktorunuza veya eczacınıza danışınız.
• Bu ilaç kişisel olarak sizin için reçete edilmiştir, başkalarına vermeyiniz.
• Bu ilacın kullanımı sırasında, doktora veya hastaneye gittiğinizde doktorunuza bu ilacı kullandığınızı söyleyiniz.
• Bu talimatta yazılanlara aynen uyunuz. İlaç hakkında size önerilen dozun dışında yüksek veya düşük doz kullanmayınız.
Bu Kullanma Talimatında:
1. EMOCLOT DI FAKTOR VIII nedir ve ne için kullanılır?
2. EMOCLOT DI FAKTOR VIII’i kullanmadan önce dikkat edilmesi gerekenler
3. EMOCLOT DI FAKTOR VIII nasıl kullanılır?
4. Olası yan etkiler nelerdir?
5. EMOCLOT DI FAKTOR VIII’in saklanması
Başlıkları yer almaktadır.
2.EMOCLOT DI FAKTOR VIII kullanmadan önce dikkat edilmesi gerekenler
EMOCLOT DI FAKTOR VIII’i aşağıdaki durumlarda KULLANMAYINIZ
Eğer,
• EMOCLOT’ın etkin maddesine veya herhangi bir yardımcı maddesine karşı aşırı duyarlılığınız varsa
Bu ilacı kullanmayınız ve bu durumunuzu doktorunuza mutlaka bildiriniz.
EMOCLOT DI FAKTOR VIII’i aşağıdaki durumlarda DİKKATLİ KULLANINIZ
Eğer,
• EMOCLOT ‘a karşı duyarlılık veya alerji şüphesi varsa
Bu uyarılar geçmişteki herhangi bir dönemde dahi olsa sizin için geçerliyse lütfen doktorunuza danışınız.
6 yaşından daha küçük çocuklarda EMOCLOT kullanımının önerilmesi ile ilgili yeterli veri bulunmamaktadır.
EMOCLOT DI FAKTOR VIII’in yiyecek ve içecek ile kullanılması
Damar içine uygulandığından aç veya tok kullanılabilir.
Hamilelik
İlacı kullanmadan önce doktorunuza veya eczacınıza danışınız.
EMOCLOT hamilelik döneminde kesin gereksinim olduğu takdirde kullanılabilir.
Tedaviniz sırasında hamile olduğunuzu fark ederseniz hemen doktorunuza veya eczacınıza danışınız.
Emzirme
İlacı kullanmadan önce doktorunuza veya eczacınıza danışınız.
EMOCLOT, emzirme döneminde kesin gereksinim olduğu takdirde kullanılabilir.
Araç ve makina kullanımı
EMOCLOT ‘ın araç ve makine kullanımı üzerine etkisi gözlenmemiştir.
EMOCLOT DI FAKTOR VIII’in içeriğinde bulunan bazı yardımcı maddeler hakkında önemli bilgiler
EMOCLOT, 66.0 mg sodyum klorür içerir. Bu durum kontrollü sodyum diyetinde olan hastalar için göz önünde bulundurulmalıdır.
Diğer ilaçlar ile birlikte kullanımı
Bugüne kadar insan plazma kaynaklı Faktör VIII konsantratının diğer ilaçlarla etkileşimleri bildirilmemiştir.
Eğer reçeteli yada reçetesiz herhangi bir ilacı şu anda kullanıyorsanız veya son zamanlarda kullandınız ise lütfen doktorunuza veya eczacınıza bunlar hakkında bilgi veriniz.
5.EMOCLOT DI FAKTOR VIII’in saklanması
EMOCLOT ‘ı çocukların göremeyeceği, erişemeyeceği yerlerde ve ambalajında saklayınız.
Buzdolabında saklayınız (2°C-8°C). Dondurmayınız. Donmuş ürünü çözüp tekrardan kullanmayınız.
Son kullanma tarihiyle uyumlu olarak kullanınız
Ambalajdaki son kullanma tarihinden sonra EMOCLOT DI FAKTOR VIII’i kullanmayınız.
Eğer ürün ve/veya ambalajında bozukluk fark ederseniz EMOCLOT ‘ı kullanmayınız.
Çevreyi korumak amacıyla kullanmadığınız EMOCLOT ‘ı şehir suyuna veya çöpe atmayınız. Bu konuda eczacınıza danışınız.
Ruhsat sahibi:
Onko İlaç San. ve Tic. A.Ş.
Koşuyolu Cad. No: 34, 34718 Kadıköy/İSTANBUL
Tel: (0216) 544 90 00
Faks: (0216) 545 59 92
e-mail: [email protected]
Üretim Yeri:
AŞAĞIDAKİ BİLGİLER BU ÜRÜNÜ UYGULAYACAK SAĞLIK PERSONELİ İÇİNDİR
Tedavi hemofili tedavisinde deneyimli bir uzman tarafından başlatılmalıdır. Ürün, intravenöz yoldan enjeksiyon veya yavaş infüzyon şeklinde uygulanır. Yerine koyma tedavisinin dozu ve süresi; Faktör VIII eksikliğinin şiddetine, kanamanın yeri ve önemi ile hastanın klinik durumuna bağlıdır.
Uygulanan Faktör VIII ünitesinin sayısı, faktör VIII ürünleri için Güncel olan WHO standartlarına bağlı olarak Uluslararası Birimler’de belirtilmiştir. Plazmadaki Faktör VIII aktivitesi yüzde olarak (normal insan plazmasına göre) ya da Uluslararası Birimde ( Plazmadaki faktör VIII için Uluslararası Standart’a göre) belirtilmiştir. Bir ünite(IU) Faktör VIII aktivitesi 1 mL normal insan plazmasında bulunan Faktör VIII miktarına eşdeğerdir. Gerekli Faktör VIII dozu 1 IU/kg Faktör VIII’in plazma Faktör VIII düzeyini % 1.5-2 yükselttiği şeklindeki ampirik bilgi esas alınarak hesaplanır.
Gerekli doz aşağıdaki formül kullanılarak tayin edilir:
Gerekli Ünite = Vücut ağırlığı (kg) x istenen Faktör VIII artışı (%) x (karşılıklı gözlenen geri alınım)
Uygulanacak miktar ve uygulama sıklığı her vakada daima klinik etkinliğe göre izlenmelidir. Aşağıdaki kanama şekillerinde Faktör VIII aktivitesi, ilgili dönem süresince belirtilen plazma aktivite seviyelerinin (normalin yüzdesi olarak) altına düşmemelidir.
Aşağıdaki tablo episodlar ve ameliyat kanamalarında dozlama kılavuzu olarak kullanılabilir.
Kanama Derecesi/ Gerekli Dozların sıklığı (saat) /
Cerrahi prosedür plazma Faktör VIII Tedavinin süresi (gün)
tipi aktivitesi (%)(IU/dL)
Kanama
Erken hemartrozis,
Kas kanaması ya da oral kanama 20-40
Daha büyük hemartrozis, 30-60 Kas kanaması ya da hematom çözülünceye
Hayatı tehdit eden kanamalar 60-100
Her 12-24 saatte tekrarlanır. En az 1 gün, ağrı ile oluşan kanama çözülünceye ya da iyileşme sağlanıncaya kadar
İnfüzyon 3-4 gün ya da daha fazla süreyle, ağrı ve akut yetersizlik kadar her 12-24 saatte bir tekrarlanmalı
İnfüzyon her 8-24 saatte bir tehlike geçinceye kadar tekrarlanmalıdır.
Ameliyat
Minör
Diş çekimi dahil 30-60 24 saatte bir, iyileşme gerçekleşinceye
kadar, en az 1 gün süresince.
Majör 80-100 İnfüzyon, yeterli yara iyileşmesi oluncaya
(pre ve post operatif) kadar her 8-24 saatte bir tekrarlanmalıdır, daha sonra faktör VIII aktivitesi %30 dan %60(30 IU/dL – 60 IU/dL) değişinceye kadar en az 7 gün süresince tedaviye devam edilir.
Tedavi süresince, uygulanacak dozun ve tekrarlayan infüzyonların sıklığının belirlenmesi için yeterli Faktör VIII seviyesinin belirlenmesi önerilir. Majör ameliyat durumunda, yerine koyma tedavisinin pıhtılaşma analizi (plazma faktör VIII analizi) yoluyla tam olarak takibi şarttır. Her bir hastanın farklı seviyelerde in vivo geri alınım ve farklı yarı-ömürler gösterecek şekilde faktör VIII’e cevabı farklı olabilir.
Profilaksi
Ağır hemofili A hastalarında kanamaya karşı uzun vadeli profilaksi için vücut ağırlığı kilo başına 20-40 IU Faktör VIII doz, 2-3 gün arayla verilmelidir. Bazı vakalarda ve bilhassa genç hastalarda, araların daha kısa yada dozların daha yüksek tutulması gerekebilir.
EMOCLOT’ın 6 yaşından küçük çocuklarda kullanımına dair mevcut veriler yeterli değildir.
Faktör VIII’e karşı antikoru (inhibitör) gelişmiş hastalar takip edilmelidir. Eğer beklenen Faktör VIII aktivitesi plazma seviyelerine ulaşılmazsa, ya da kanama uygun bir doz ile kontrol altına alınamazsa, bir Faktör VIII inhibitörünün olup olmadığını saptamak için bir test yapılmalıdır. Yüksek inhibitör seviyeli hastalarda faktör VIII tedavisi etkili olmayabilir ve diğer terapötik tercihler düşünülmelidir. Bu gibi hastaların tedavisi hemofili hastaların tedavisinde deneyimli uzmanlara yönlendirilmelidir.
Uygulama şekli:
Flakon içeriğindeki toz haldeki etken madde aşağıda anlatıldığı şekilde çözündürülür.
Ürün, intravenöz yoldan enjeksiyon veya yavaş infüzyon şeklinde uygulanır.
İntravenöz enjeksiyon yapılıyorsa, nabız hızlandığı takdirde enjeksiyonu yavaşlatmak ya da durdurmak suretiyle uygulamanın başında 3-5 dakika süre ile hastanın nabzının takip edilmesi önerilir.
Uygulamanın hızı her bir hasta için değerlendirilmelidir. Tozun çözücü ile rekonstitüe edilmesi,
1. Toz halde etken madde içeren flakon ve çözücüyü oda sıcaklığına getirin;
2. Toz etken madde içeren flakon ve çözücü flakonun kabını çıkartın;
3. İki flakon tıpasının yüzeyini alkol ile temizleyin;
4. Başlığı sıyırarak aparatın ambalajını açın; iç kısma dokunmamaya dikkat edin (Şekil A);
5. Aparatı ambalajından çıkarmayın;
6. Aparat kutusunu baş aşağı çevirin ve çözücü flakon tıpasına doğru plastik sivri ucu yerleştirin ( Şekil B);
7. Aparatı serbest bırakmak için aparat kutusunun kenarını tutun ve çekin ( Şekil C);
8. Aparatı çözücü flakonuna bağlı bırakın; sistemi ters çevirin böylece çözücü flakonu aparatın üstünde olur;
9. Toz flakon tıpasına doğru diğer sivri uçlu plastiği yerleştirin; toz flakondaki vakum, çözücüyü toz flakonun içine çekecektir ( Şekil D);
10. Çözünme tamamlanıncaya kadar yavaşça çalkalayınız ( Şekil E); ürünün tamamen çözündüğünden emin olun, diğer türlü etken madde aparatın filtresinden geçmeyecektir.
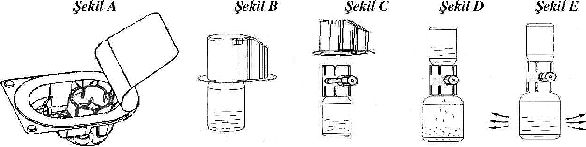
Sulandırma süresi 3 dakikadan daha kısadır.
Çözücü sıcak su banyosu içinde ısıtılarak, flakonu sulandırdıktan sonra 37oC’nin üstünde olmamak kaydıyla ısıtmaya devam ederek liyofilize maddenin daha çabuk çözülmesi sağlanabilir.
Eğer toz tamamen çözülmezse filtrasyon sırasında aktivite kaybı olur. Flakonun iç yüzeylerine çözücünün yavaşça akması sağlanarak köpük oluşumu önlenir.
Çözeltinin uygulanması Çözelti berrak veya hafif opelesan.
Ürün sulandırmadan sonra az miktarda küçük tanecik veya partikül içerebilir.
Çözeltide katı parçacık olup olmadığını veya uygulamadan önce renginin değişip
değişmediğini inceleyin. Bulanık veya tortu olan çözeltileri kullanmayınız.
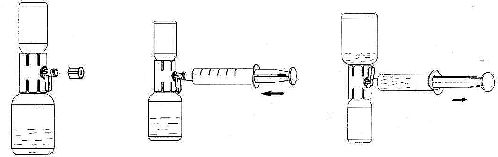
1. Rekonstitüe çözeltiyi içeren toz flakona doğru aparat kapağını çekin ve onu kaplayan kabı uzaklaştırın ( Şekil F);
2. Şırıngayı hava ile doldurun, pistonu geri çekin, aparata tutturun ve havayı rekonstitüe çözeltiyi içeren toz flakonun içine enjekte ediniz ( Şekil G);
3. Pistonu bırakın, sistemi ters çevirin böylece toz flakonu aparatın üstündedir ve yavaşça piston geri çekilerek konsantre şırınganın içine çekilir ( Şekil H);
4. Kapağı yavaşça orijinal durumuna çevirin ve şırıngayı çıkartın.
5. Şırıngaya kelebek iğnesini yerleştirin ve intravenöz olarak infüze veya yavaşça enjekte edilir.
Şekil F
Şekil G
Şekil H
Flakonlar bir kere açıldıktan sonra, içerik derhal kullanılmalıdır. Sulandırılan çözelti ve şırınganın içine transfer edilen derhal kullanılmalıdır. Flakon içeriği tek bir uygulama için kullanılmalıdır.
Etiket üzerinde belirtilmiş olan son kullanma tarihi geçmiş ürün kullanılmamalıdır. Arta kalan kullanılmamış çözelti uygun bir şekilde yok edilmelidir.
2.EMOCLOT DI FAKTOR VIII nedir ve ne için kullanılır?
• EMOCLOT kullanılmadan önce sulandırılan enjeksiyonluk çözeltidir ve antihemorajikler grubundan olan kan koagülasyon Faktör VIII'dir.
• EMOCLOT enjeksiyon için toz ve çözücü içerir. Toz içeren tip I elastomer kapaklı nötral tip I cam flakon; çözücü içeren tip I elastomer kapaklı nötral tip I cam flakon; pirojensiz, steril, tek kullanımlık set, sulandırma için üç yollu tıbbi cihaz, enjeksiyon için bir şırınga ve PVC tüplü kelebek iğnesi içerir.
• EMOCLOT, hemofili A hastalarında (konjenital faktör VIII yetmezliği) kanamanın profilaksi ve tedavisinde, edinilmiş faktör VIII yetmezliğinde, faktör VIII'e karşı antikor gelişmiş hemofili hastalarının tedavisinde kullanılır.
3.EMOCLOT DI FAKTOR VIII nasıl kullanılır ?
Uygun kullanım ve doz/uygulama sıklığı için talimatlar
'Doktorunuz hastalığınıza bağlı olarak ilacınızın dozunu belirleyecek ve size uygulayacaktır.'
Uygulama yolu ve metodu
Damar içine (intravenöz) uygulanır.
Çocuklarda kullanımı
Yaşlılarda kullanımı
Yaşlılarda kullanımı
Yaşlılarda kullanımı
Özel kullanım durumları
Böbrek/ Karaciğer yetmezliği:
EMOCLOT'ın böbrek/karaciğer yetmezliği bulunmamaktadır.
olan hastalarda kullanımına ilişkin veri
Eğer etkisinin çok güçlü veya zayıf olduğuna dair bir izleniminiz var ise doktorunuz veya eczacınız ile konuşunuz.
Kullanmanız gerekenden daha fazla EMOCLOT DI FAKTOR VIII kullanırsanız
EMOCLOT 'dan kullanmanız gerekenden fazlasını kullanmışsanız bir doktor veya eczacı ile konuşunuz.
EMOCLOT DI FAKTOR VIII'i kullanmayı unuttuysanız
Unutulan dozları dengelemek için çift doz almayınız.
EMOCLOT DI FAKTOR VIII ile tedavi sonlandırıldığında oluşabilecek etkiler
Herhangi bir veri bulunmamaktadır.
4.Olası yan etkiler nelerdir ?
Tüm ilaçlar gibi EMOCLOT DI FAKTOR VIII’in içeriğinde bulunan maddelere duyarlı olan kişilerde yan etkiler olabilir.
Aşağıdakilerden biri olursa, kullanmayı durdurunuz ve DERHAL doktorunuza bildiriniz veya size en yakın hastanenin acil bölümüne başvurunuz:
• Kalp atımımın hızlanması
• Hırıltılı solunum
• Ciltte döküntüler veya kaşıntı
• Göğüste sıkışma hissi
• Titreme
• Ateş yükselmesi
Bunlar hepsi çok ciddi yan etkilerdir. Görülme sıklığı seyrektir.
- Eğer bunlardan biri sizde mevcut ise, sizin karşı ciddi alerjiniz var demektir. Acil tıbbi müdahaleye veya hastaneye yatırılmanıza gerek olabilir.
Aşağıdakilerden herhangi birini fark ederseniz hemen doktorunuza bildiriniz veya size en yakın hastanenin acil bölümüne başvurunuz:
• Baş ağrısı
• Karıncalanma hissi
• Tansiyon düşüklüğü
• Sıcak basması
• Alerjik reaksiyonlar
• Huzursuzluk hissi
• Bulantı
• Kusma
Bunlar hepsi ciddi yan etkilerdir. Acil tıbbi müdahale gerekebilir. Ciddi yan etkiler çok seyrek görülür.
Aşağıdakilerden herhangi birini fark ederseniz doktorunuza söyleyiniz:
• Enjeksiyon yerinde yanma ve kaşıntı Bunlar hafif yan etkileridir.
Yan etkilerin raporlanması
Kullanma Talimatında yer alan veya almayan herhangi bir yan etki meydana gelmesi durumunda hekiminiz, eczacınız veya hemşireniz ile konuşunuz. Ayrıca karşılaştığınız yan etkileri www.titck.gov.tr sitesinde yer alan “İlaç Yan Etki Bildirimi“ ikonuna tıklayarak ya da 0 800 314 00 08 numaralı yan etki bildirim hattını arayarak Türkiye Farmakovijilans Merkezi (TÜFAM)‘ne bildiriniz. Meydana gelen yan etkileri bildirerek kullanmakta olduğunuz ilacın güvenliliği hakkında daha fazla bilgi edilnilmesine katkı sağlamış olacaksınız.
